Cho hai phương trình nhiệt hóa học sau:
CO(g) + ½ O2(g) → CO2(g) Δr\(H^0_{298}\) = -283,00 kJ (1)
H2(g) + F2(g) → 2HF(g) Δr\(H^0_{298}\) = -546,00 kJ (2)
So sánh nhiệt giữa hai phản ứng (1) và (2). Phản ứng nào xảy ra thuận lợi hơn?
Cho hai phương trình nhiệt hóa học sau:
C(s) + H2O(g) \(\underrightarrow{t^o}\) CO(g) + H2(g) Δr\(H^0_{298}\) = +131,25 kJ (1)
CuSO4(aq) + Zn(s) → ZnSO4(aq) + Cu(s) Δr\(H^0_{298}\) = -231,04 kJ (2)
Trong hai phản ứng trên, phản ứng nào thu nhiệt, phản ứng nào tỏa nhiệt?
Cho hai phản ứng đốt cháy:
(1) C(s) + O2(g) → CO2(g) ${\Delta _r},H_{298}^0$ = -393,5 kJ
(2) 2Al(s) + 3/2 O2(g) → Al2O3(s) ${\Delta _r},H_{298}^0$ = -1675,7 kJ
Với cùng một khối lượng C và Al, chất nào khi đốt cháy tỏa ra nhiều nhiệt hơn?
Giả sử: 1 gam C và Al
+ 1 gam C có 1/12 mol
1 mol C : ${\Delta _r},H_{298}^0$ = -393,5 kJ
1/12 mol C ${\Delta _r},H_{298}^0$ = -32,79 kJ
+ 1 gam Al có 1/27 mol
2 mol Al : ${\Delta _r},H_{298}^0$= -1675,7 kJ
1/27mol Al : ${\Delta _r},H_{298}^0$= -31,03 kJ
⇒ Với cùng một khối lượng C và Al, C khi đốt cháy tỏa ra nhiều nhiệt hơn.
Cho phương trình nhiệt hóa học sau:
SO2(g) + ½ O2(g) \(\underrightarrow{t^o,V_2O_5}\) SO3(g) Δr\(H^0_{298}\) = -98,5 kJ
a) Tính lượng nhiệt giải phóng ra khi chuyển 74,6 g SO2 thành SO3
b) Giá trị Δr\(H^0_{298}\)của phản ứng: SO3(g) → SO2(g) + ½ O2(g) là bao nhiêu?
Cho phản ứng sau:
S(s) + O2(g) \(\underrightarrow{t^o}\) SO2(g) Δf\(H^0_{298}\)(SO2,g) = -296,80 kJ/mol
Cho biết ý nghĩa của giá trị Δf\(H^0_{298}\)(SO2,g)

Phương trình nhiệt hóa học giữa nitrogen và oxygen như sau:
N2(g) + O2(g) → 2NO(g) Δr\(H^0_{298}\)= +180 kJ
Kết luận nào sau đây đúng?
A. Nitrogen và oxygen phản ứng mạnh hơn khi ở nhiệt độ thấp
B. Phản ứng tỏa nhiệt
C. Phản ứng xảy ra thuận lợi ở điều kiện thường
D. Phản ứng hóa học xảy ra có sự hấp thụ nhiệt năng từ môi trường
Xét phản ứng trong giai đoạn đầu của quá trình Ostwald:
4NH3(g) + 5O2(g) (Pt, t°) → 4NO(g) + 6H2O(g)
a) Tính Δ\(rH^0_{298}\) của phản ứng trên và cho biết phản ứng là toả nhiệt hay thu nhiệt? Có thể tận dụng nhiệt lượng này để làm gì?
Biết nhiệt tạo thành chuẩn của NH3(g), NO(g) và H2O(g) lần lượt là -45,9 kJ/mol; 90,3 kJ/mol và -241,8 kJ/mol.
b) Tính năng lượng liên kết trong phân tử NO. Biết năng lượng liên kết N─H, O═O, O─H lần lượt là 386 kJ/mol, 494 kJ/mol và 459 kJ/mol.
5. Giá trị \(\Delta_rH^0_{298}\) của phản ứng sau là bao nhiêu kJ?
½ CH4(g) + O2(g) → ½ CO2(g) + H2O(l)
Giá trị ${\Delta _r}H_{298}^0$ của phản ứng sau là bao nhiêu kJ?
½ CH4(g) + O2(g) → ½ CO2(g) + H2O(l)
½ CH4(g) + O2(g) → ½ CO2(g) + H2O(l) ${\Delta _r}H_{298}^0 = \frac{{ - 890,36}}{2} = - 445,18kJ$
Câu 5. Methane là thành phần chính của khí thiên nhiên. Xét phản ứng đốt cháy methane:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) Δr\(H^0_{298}\)= -890,3 kJ
Biến nhiệt tạo thành chuẩn của CO2(g) và H2O(l) tương ứng là -393,5 và -285,8 kJ/mol.
Hãy tính nhiệt tạo thành chuẩn của khí methane.
Gọi nhiệt tạo thành chuẩn của khí methane là x
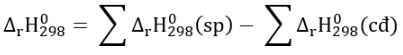
\(\rightarrow\) -890,3 = 2.(-285,8) -393,5 - x - 2.0
\(\rightarrow\) x = – 74,8 kJ/mol